
2- Les techniques et les diverses lois impliquées dans cette discipline
La physique est un domaine inaliénable de la plongée. C'est pourquoi on peut retrouver dans ce sport un certain nombre de lois et de techniques permettant de comprendre certaines consignes données.
Tout d'abord, la pression est une notion utilisée de façon permanente en plongée. De plus, la pression est une force qui s'applique sur une surface. C'est pourquoi la pression est égale à la force divisée par la surface ( P=F : S ).
L'unité légale de la pression est le Pascal (Pa) mais en plongée celle-ci est souvent exprimée en bar (b). La pression est d'autant plus grande quand la force exercée est grande et lorsque la surface sur laquelle elle s'exerce est petite.
La pression relative est quant à elle la pression exercée par le poids de l'eau, et celle-ci augmente quand la surface sur laquelle elle s'exerce est petite.
La pression absolue différente de ces deux dernières nous informe que tout corps plongé dans l'eau subit en plus de la pression relative, la pression atmosphérique ( même si le corps n'est pas en contact direct avec l'air). De plus la pression atmosphérique est environ égale à 1bar au niveau de la mer et est constante. La pression absolue est donc la somme de la pression relative et atmosphérique.
Exemple :

C'est donc pour cela que nous pouvons alors nous interroger sur le principe Archimède.
En effet, la première chose sur laquelle un jeune plongeur peut s'interroger est sur sa capacité à flotter dans l'eau. Cette flottabilité sera expliquée par le physicien Archimède qui donnera son nom à cette loi : « Tout corps plongé dans un fluide subit de la part de celui-ci une poussée verticale dirigée de bas en haut égale au poids du volume du fluide déplacé. ». Cela signifie qu'un objet exerce un poids vertical de haut en bas mais qu’au contraire le liquide exerce un poids de bas en haut qui est dû à une pression plus importante en profondeur qu’en surface.
De plus, si un objet est plus lourd que le volume du liquide déplacé, tel qu’un objet en béton, le poids exercé vers le bas sera plus important que celui exercé vers le haut, l'objet coulera alors et au contraire un objet léger comme le bois flottera car le poids dirigé vers le haut sera plus important. Cela explique que nous pouvons contrôler notre flottabilité en gonflant ou dégonflant le gilet stabilisateur.
Comme nous l'avons vu précédemment, la pression est plus importante en profondeur qu’en surface. Pour démontrer cela nous avons réalisé une expérience :
Matériel utilisé :
• Une éprouvette graduée remplie d’eau à 250ml
• Du papier millimétré
• Un tube
• Un pressiomètre
adresse url:
https://www.youtube.com/watch?v=-lWlDUMVthE
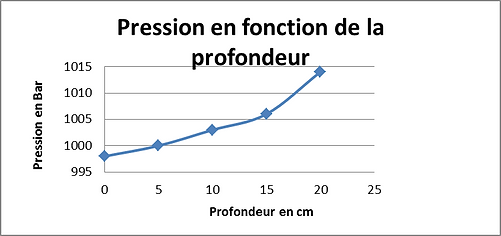
Pour cette expérience nous avons utilisé une éprouvette que nous avons remplie avec de l’eau jusqu’à 250ml. Pour plus de précision nous avons scotché sur celle-ci une bande découpée de papier millimétré pour pouvoir ainsi mesurer la profondeur. Nous avons relié un tube au pressiomètre que nous avons plongé dans l’éprouvette à mesure différente. Ainsi on constate que plus le tube est profond plus la pression augmente.
Voici nos résultats de l'expérience sous forme de graphique
Toujours en lien avec cette certaine pression on peut en effet retrouver la loi d'Henry. Cette loi nous informe que « à température donnée et à saturation, la quantité de gaz dissout dans un liquide est proportionnelle à la pression exercée par ce gaz sur le liquide ».
Néanmoins, il est bon de savoir qu’en plongée, on retrouve avec l’azote le même phénomène qu’avec une bouteille de boisson gazeuse. En effet, on peut observer une différence d’eau liquide contenu dans celle-ci. Lorsque cette bouteille sera ouverte les bulles vont subitement apparaître et remonter à la surface. Ce phénomène de gaz est le même que celui qui se dissout dans l’organisme lors de la descente et également durant le temps passé au fond. Lors de la remontée, ce gaz se dissout et reprend sa forme gazeuse et est éliminé lors de l’expiration tout au long de la phase de décompression. De plus, le physicien et chimiste John Dalton précise que la présence d'un gaz nocif dans l'air que l'on respire peut être soit inoffensif, soit provoquer des malaises, ou même être fatale. Tout dépend de la quantité de gaz qui s'y trouve. Le fait qu'il soit mélangé à un autre gaz n'empêche pas ses effets. Suite à ses observations, Dalton énonce la loi suivante qui dit que "la pression partielle d'un constituant d'un mélange gazeux est égale à la pression qu'il aurait s'il remplissait seul le volume occupé par le mélange".
Cette loi a donc un impact important sur le plongeur, particulièrement en ce qui concerne sa sécurité, le remplissage des bouteilles et le réglage de son matériel.
Pour revenir à la loi de Henry, cette quantité de gaz dissoute dans le liquide est appelée la tension du gaz.
Si les conditions extérieures restent stables, il s'établit entre la pression du gaz au-dessus du liquide et la tension du gaz dans ce liquide un équilibre. On dit alors que le liquide est à saturation.
Si on augmente la pression du gaz alors le liquide passe à un état de sous-saturation.
Si on diminue la pression du gaz le liquide passe en sur-saturation.
Dans ces deux cas, des molécules de gaz passeront ou s’échapperont alors du liquide jusqu’à atteindre à nouveau la saturation.
Si la pression baisse rapidement, il peut se former dans le liquide des bulles.
Ce qui est à retenir:
Saturation : Pression = Tension
Sous-saturation : Pression > Tension
Sur-saturation: Pression < Tension
Cette loi d'Henry nous amène donc à comprendre la technique des paliers de décompression. Cette technique est utilisée pour éliminer une quantité d'Azote suffisante et donc éviter la formation de ces bulles dans le sang notamment. Ce procédé consiste à marquer une pause à différentes profondeurs pendant un certain temps. Cette profondeur ainsi que la durée de la pause dépend de la profondeur à laquelle nous plongeons mais aussi du temps passé sous l'eau. Des tables de décompression ont donc été mises en place en 1990 par la Marine nationale dans le but de fixer la durée des paliers à effectuer ainsi que son niveau de profondeur pour respecter les procédures de décompression adéquates.


Exemples: - Pour une profondeur de 25m et une durée de plongée de 35min un palier de 5min est obligatoire à 3m.
- Pour une profondeur de 28m et une durée de plongée de 20min un palier de 1min est obligatoire à 3m.
- Pour une profondeur de 30m et une durée de plongée de 45min un premier palier de 1min à 6m suivit d'un second à 3m d'une durée de 31min sont obligatoires.
Néanmoins, une courbe de sécurité a été élaborée suite à cela pour permettre au plongeur d'explorer les fonds marins à des profondeurs spécifiques sans pour autant devoir effectuer des paliers lors de la remontée:

La dernière loi qu'un plongeur doit connaître est en l'occurrence la loi de Boyle-Mariotte. Cette loi nous informe qu'à température constante, pour une quantité de matière donnée de gaz, le produit de la pression P par le volume V de ce gaz ne varie pas, cela signifie alors que : P x V= constante.
On peut alors déduire de cette loi qu’à une température constante, le volume occupé par une quantité de matière donnée de gaz ne dépend que de la pression. Il ne dépend pas de la nature du gaz. De plus, suivant la loi de Boyle-Mariotte, la diminution de la pression s’accompagne donc d’une augmentation du volume de l’air contenu dans les poumons. C’est pourquoi si le plongeur bloque sa respiration lors de la remontée, l’air continu à se dilater jusqu'à atteindre la limite d’élasticité des poumons. Il est donc dangereux de retenir sa respiration lors de la remontée.
On peut ensuite vérifier cette loi par le biais d'une expérience:
Matériel utilisé :
-un pressiomètre
-une seringue (qui est remplie d’air)
adresse url:
Après avoir relié la seringue au pressiomètre, on appuie sur celle-ci dans le but de diminuer l’air en le comprimant. On relève des mesures du pressiomètre tous les 5 ml d’air.
On obtient donc ce graphique:

On constate que plus le volume d’air de la seringue diminue, plus la pression augmente, et inversement. On a donc démontré la loi de Boyle-Mariotte prouvant que Pression x Volume = Constante.
Si Joël sait maintenant d'où viennent les effets de la pression ou comment se servir des tables de paliers de décompression, Il appréhende sa sortie et peut se demander lequels de ses organes sont menacés et aussi quels est leurs réels rôles et fonctionnement ( si il s'avère que cela paraît logique, il n'est pas aussi évident d'expliquer cela clairement)